Cas clinique – Baisse de la vision soudaine
Opto-MAG 10 janvier 2023, Diana Morais de Almeida

Des progrès scientifiques ont permis d’en savoir plus sur la physiopathologie, le diagnostic et les stratégies thérapeutiques d’une multitude de maladies de la rétine.
Comme connu, certaines maladies ayant des répercussions sur la rétine sont liées à des processus physiologiques dérivés d’altérations systémiques. Des niveaux élevés d’hormones de stress, telles que le cortisol et les catécholamines, ont été associés à certaines altérations de la rétine, plus spécifiquement de la perméabilité du réseau vasculaire choroïdien 1. Même si de nombreux autres éléments constituent un risque particulier de certaines maladies rétiniennes, le stress psychologique devrait également avoir sa place dans l’analyse des cas spécifiques d’une baisse de la vision.
Étude de cas
Une femme de 46 ans se présente aux urgences en décrivant un scotome relatif central à l’OG, depuis 3 jours. En absence d’antécédents ophtalmiques ni d’historique familiale, la patiente révélait une hypothyroïdie non traitée et des problèmes hormonaux récents avec une prise de cortisone, une semaine avant, pour des investigations d’un test sanguin. Des questions doivent se poser aussi sur les circonstances sociales. Des événements atypiques qui provoquent du stress et de l’anxiété peuvent avoir un impact sur la santé, notamment sur la fonction visuelle. La patiente a relevé une période de stress récemment à cause des problèmes familiaux.
Évaluation initiale
La meilleure AV de loin à l’OD était de 1.6 sans correction et à l’OG de 1.25 non améliorable. La pression intraoculaire ainsi que l’examen du segment antérieur étaient dans la norme. Parmi les tests fonctionnels, qui peuvent orienter et valider notre évaluation, se trouvent : – – – L’Ishihara : une dyschromatopsie légère a été détectée. La vision des couleurs est souvent altérée dans une atteinte de la rétine. La Grille d’Amsler : des scotomes ou métamorphopsies doivent être recherchés pour une suspicion de maculopathie. Des métamorphopsies centrales ont été décelées lors de l’examen et un scotome relatif central. Mesure de la sensibilité aux contrastes qui est souvent diminuée
À l’examen du segment postérieur, une altération du reflet maculaire à l’OG se présentait avec une forme circulaire impliquant la fovéa qui nous montre un soulèvement bulleux de la rétine. L’OD ne révélait aucun problème.
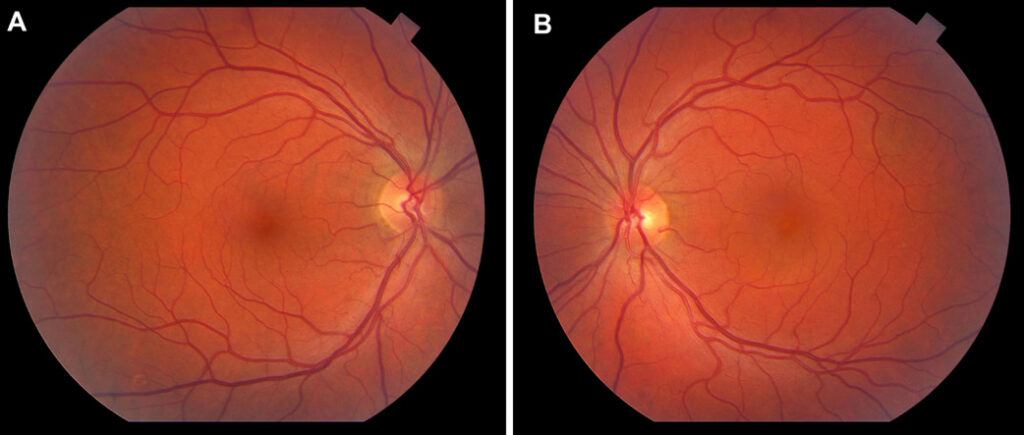
Figure 1. Image 2 représentative d’un FO dilaté avec les mêmes caractéristiques. A) L’OD présente un reflet fovéolaire normal. B) L’OG révèle une absence de reflet fovéolaire, plus pâle avec un soulèvement de la zone de la macula indiqué par les veines et artères au tour qui remontent.
Examen clinique
Un OCT est le premier examen complémentaire conseillé comme guide pour la suite de la prise en charge.
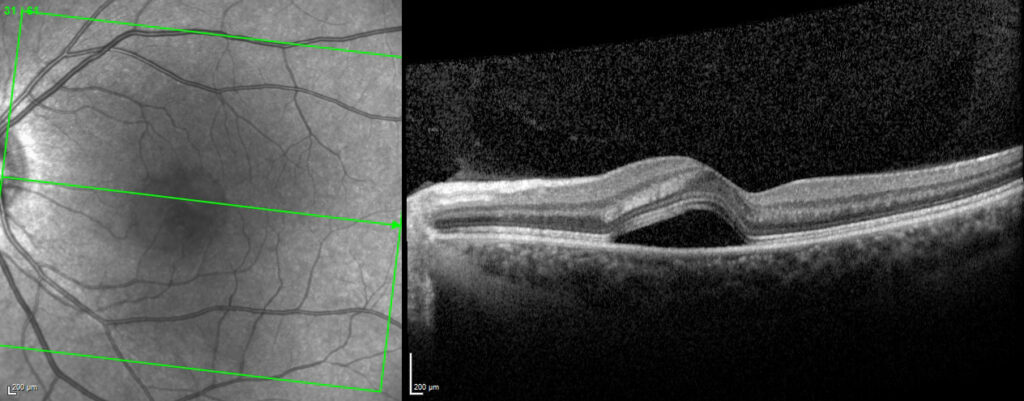

Figure 2. (A) L’OCT de l’OG montre un décollement et accumulation de liquide sous la rétine neurosensoriel dans la zone de la macula, avec une représentation en 3D du soulèvement bulleux(B)
À l’aide des évidences caractérisées à l’OCT et sans autres problèmes oculaires ou troubles systémiques, une forte suspicion d’une choriorétinopathie séreuse centrale (CRSC) est considérée.
Diverses pathologies rétiniennes ont un profil similaire au diagnostic d’une CRSC en raison des caractéristiques générales au FO dilaté et d’imagerie OCT.
Principaux diagnostics différentiels 3 :
- DMLA néovasculaire du type 1
- Vasculopathie polypoïdale choroïdienne
- Optic disc pit
- DMLA néovasculaire du type 1
- Vasculopathie polypoïdale choroïdienne
Diagnostic structurel
Pour aider à l’exclusion de ces pathologies et à la confirmation du diagnostic d’une CRSC aiguë, il s’avère nécessaire d’analyser certains examens, comme un examen attentif du fond d’oeil dilaté, les antécédents complets du patient et l’identification de tout facteur de risque commun de CSCR.
1. Une angiographie
Bien que l’étiologie et la pathogénie exactes soient encore inconnues, la CRSC reste une des plus courantes maladies rétiniennes qui peut entraîner une déficience visuelle avec une baisse de vision soudaine1. La CRSC appartient au spectre des pathologies associées à la pachychoroïde caractérisée par un dysfonctionnement de la choriocapillaire et de la choroïde. Est une maladie qui se manifeste par des lames de sérosité (qualifiées de décollements séreux sous rétiniens) qui sont en lien avec une hyperperméabilité des vaisseaux de la couche vasculaire choroïdienne. Le contenu liquidien du sang (le plasma) infiltre l’espace sous rétinien à travers les parois vasculaires devenues perméables et provoque le DSR.
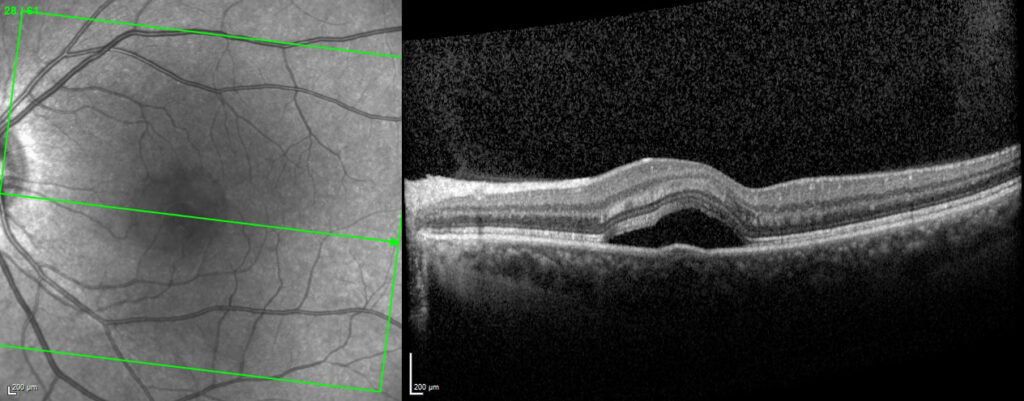
Figure 3. Coupe d’OCT qui montre un DEP en parafovéolaire (B).
Les images en mode EDI (Enhanced Depth Imaging) sont importantes et permettent de visualiser les couches plus postérieures qui correspondent aux gros vaisseaux choroïdiens. Une épaisseur choroïdienne sous-fovéale de > 300 μm a été considérée comme une choroïde épaisse et peut avoir une corrélation avec la CRSC. 4
AF (image en autofluorescence): utile pour aider à différencier si CRSC chronique qui se révèle souvent par une disposition des plages hyperautofluorescentes en coulée gravitationnelle . Cette manifestation implique que la CSCR est présente depuis un certain temps.
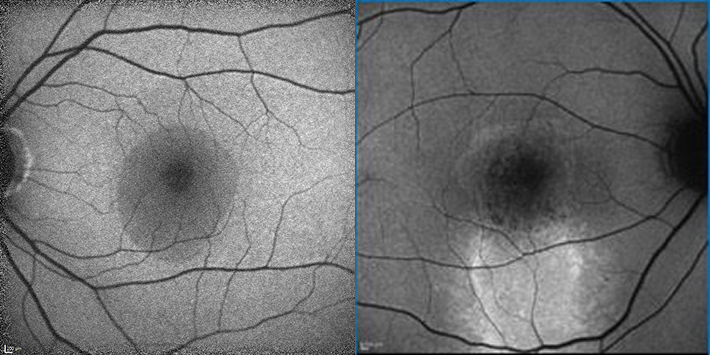
Fig. 4 A) image en autofluorescence de l’OG de la patiente montrant une probable CRSC aiguë avec une hypo-autofluorescence de la zone du décollement séreux (liquide bloque le passage de la lumière) vs (B) image AF comparative d’une CRSC chronique. Les zones d’hyper-autofluorescence montrant le liquide sous-rétinien chronique qui descend et ces taches hyper-autofluorescentes peuvent correspondre à des débris/précipités des photorécepteurs.
2. OCT-EDI-AF:
L’angiographie OCT (OCT-A) est une méthode non invasive d’imagerie du réseau vasculaire rétinien et choroïdien qui aide à l’analyse des caractéristiques d’un flux sanguin anormal si existant. Dans ce cas, cet examen nous permet d’exclure une complication néovasculaire dans la zone du DEP. Le recours à cet examen se prouve important dans la présence d’un DEP irrégulier, habituellement indiqué comme FIPED -flat irregular pigment epithelium detachment, qui est associé à des CRSC chroniques.
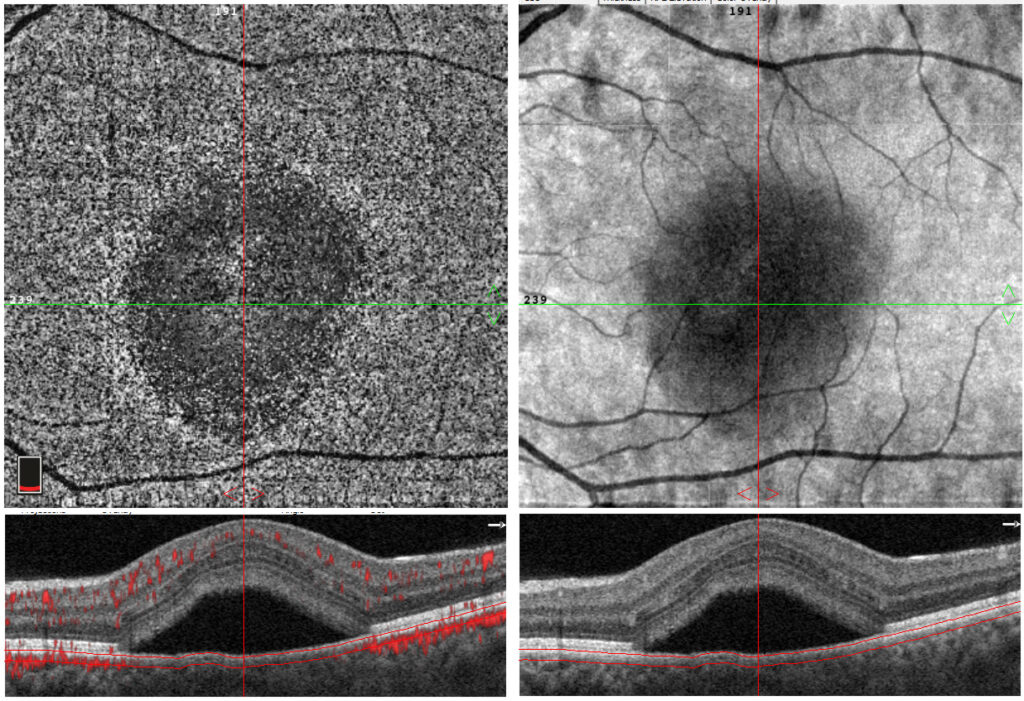
Fig. 5 OCT-A réalisé à 1 mois de suivi. Dans l’analyse de la choriocapillaire, le réseau vasculaire profond ne montre pas de néovascularisation,
3 Une angiographie à la fluorescéine (FA) et au vert d’indocyanine (ICG) aide à savoir si la condition est plus localisée ou diffuse. Aide à localiser des points de fuite ainsi qu’à mettre en évidence une dilatation des vaisseaux choroïdiens.
Pour cette raison elle est conseillée seulement si :
- Suspicion de CRSC chronique ou récidivante
- Diagnostic incertain/si présentation atypique
- Exclure maladies infectieuses
- Suivi forme chronique
- Assister au traitement par photocoagulation au
- laser ou photothérapie dynamique
PLAN DE SUIVI
En 1ère intention : expliquer les risques de récidive, réduire le stress, éviter la prise de corticoïdes, contrôler les facteurs de risque, autosurveillance avec la grille d’Amsler et observer.
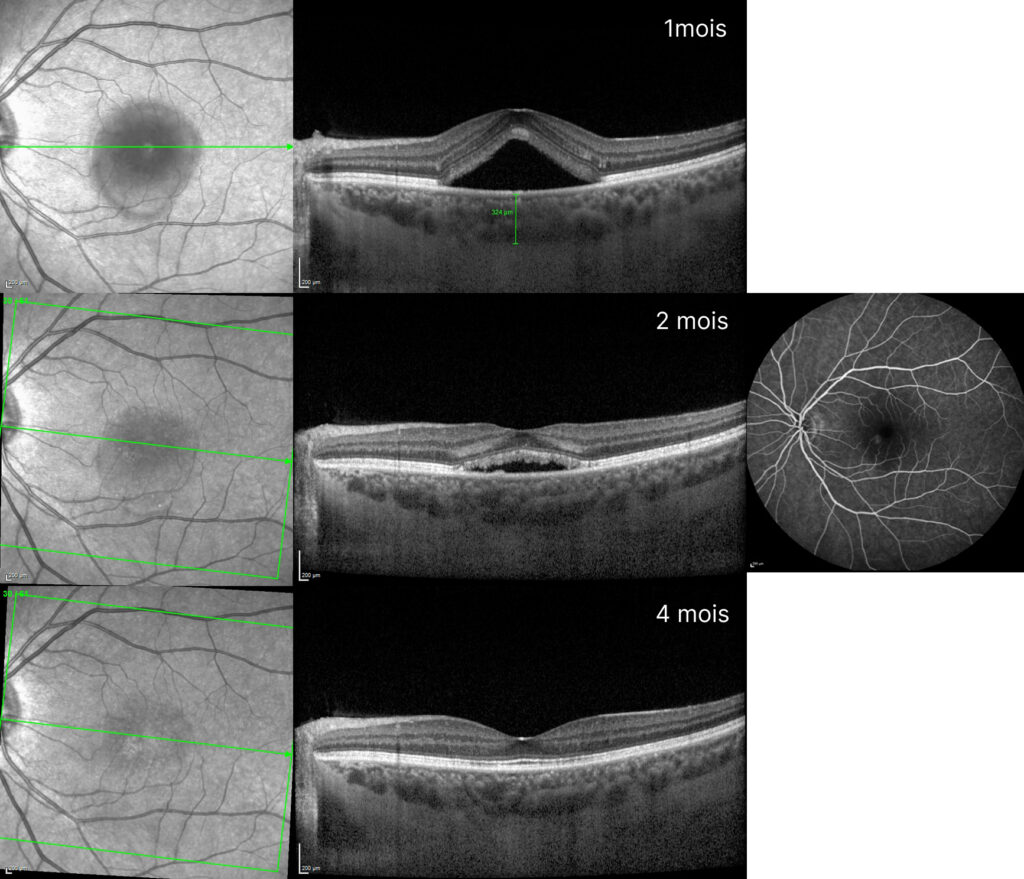
Fig. 5 A) Coupe OCT en EDI lors du suivi a 1 mois, qui montre une nette augmentation du liquide sous rétinien (LSR). Mesure de l’épaisseur de la choroïde de 324μm. Les corticoïdes n’étaient pas repris par la patiente, mais de fortes périodes de stress étaient encore en cours. En raison de ces événements, la patiente était conseillée de revenir dans un mois avec un rappel de l’importance de la réduction du stress. B) Résolution partielle spontanée du LSR à 2 mois avec une image de FA aux temps précoces, qui était déjà prévue pour suspicion d’une CRSC récidivante, montrant le point de fuite correspondant au DEP. C) Résorption complète du liquide au suivi de 4 mois.
Discussion
1. Pathophysiologie: Bien que l’étiologie et la pathogénie exactes soient encore inconnues, la CRSC reste une des plus courantes maladies rétiniennes qui peut entraîner une déficience visuelle avec une baisse de vision soudaine1.local du point de fuite du liquide séreux.
La CRSC appartient au spectre des pathologies associées à la pachychoroïde caractérisée par un dysfonctionnement de la choriocapillaire et de la choroïde. Est une maladie qui se manifeste par des lames de sérosité (qualifiées de décollements séreux sous rétiniens) qui sont en lien avec une hyperperméabilité des vaisseaux de la couche vasculaire choroïdienne. Le contenu liquidien du sang (le plasma) infiltre l’espace sous rétinien à travers les parois vasculaires devenues perméables et provoque le DSR.
2. Facteurs de risque La prévalence est plus élevée parmi les hommes entre 30 et 50 ans qui ont une charge de travail importante. La surcharge mentale, comme conséquence, peut être une source de stress psychologique difficile à gérer entrainant une augmentation du taux des hormones de stress, en particulier les corticostéroïdes et les catécholamines. 5
Des évidences démontrent l’influence génétique, mais la corticothérapie est le facteur déclenchant ou aggravant le mieux documenté, quel que soit le mode d’administration (intranasale, inhalée, topique, intraarticulaire, orale, intraveineuse, etc. 6
D’autres facteurs de risque communs incluent : la HTA non contrôlée, la dépression, le tabagisme, l’apnée du sommeil, la grossesse, le travail de nuit et l’infection à Helicobacter pylori 9
3. Examen clinique BAV modérée unilatérale : mesurer l’av de près renforce la suspicion des problèmes rétiniens ; une hypermetropisation peut survenir initialement Micropsies +/- métamorphopsies et un scotome relatif peuvent être décelés à la grille d’Amsler
Diminution des contrastes est évaluée avec la mesure de la sensibilité aux contrastes : on peut avoir un patient qui remarque plus facile à lire sur un contraste inversé Dyschromatopsie : test Ishihara avec des défauts surtout dans l’axe bleu-jaune Si extrafovéolaire peut être asymptomatique
LOCT : Typiquement la CRSC se présente comme un décollement séreux localisé de la rétine neurosensorielle impliquant la région de la macula sans hémorragies sous-rétiniennes ou exsudats lipidiques. Les bords du décollement séreux sont inclinés et se fondent progressivement dans la rétine normalement attachée au pôle postérieur. Il est parfois associé à un ou plusieurs DEP séreux qui peuvent se présenter sans inclure la macula. Si le fluide est hors de la fovéa et en supérieur, le suivi doit être raccourci pour détecter une éventuelle descente du liquide à cause de l’effet de la gravité.
D’autres facteurs de risque communs incluent : la HTA non contrôlée, la dépression, le tabagisme, l’apnée du sommeil, la grossesse, le travail de nuit et l’infection à Helicobacter pylori. 9
4. Évolution/Pronostic
CRSC aiguë :
- Difficile à estimer, la résolution spontanée peut être considérée entre 80-90% des patients
- Récupération totale de la vision de 1 à 3 mois sans dégénération des photorécepteurs/EPR et une diminution
- des contrastes et altération des couleurs qui peut persister quelques mois
- Pas d’évidence clinique d’utiliser un traitement
- 5 à 50% des patients peuvent avoir une récidive quelques mois ou années plus tard choroïdiens.
CRSC chronique :
- 10% des patients
- Souvent bilatérale
- Débute à un âge plus tardif (35-55 ans)
- Période d’exacerbation et de rémission
- Après l’exclusion d’une CNV (néovascularisation choroïdienne), le traitement à considérer est -Photothérapie dynamique (PDT) si le point fuite est en jouxta/rétrofovéolaire
-Photocoagulation au laser, sur le point de fuite en extrafovéolaire
Conclusion
Il existe de nombreux facteurs à prendre en compte lors de la classification de la CRSC et divers tests permettant d’identifier les signes de la CRSC. Une classification de la CRSC est proposée par l’American Academy of ophtalmology en utilisant des critères basés sur des modifications de l’EPR et du DSR à partir de l’imagerie multimodale. 7
Le traitement et le suivi de la CRSC doivent être adaptés à chaque patient, en fonction des facteurs tels que la vision, les altérations de la rétine/EPR et d’éventuels épisodes antérieurs.
De nouvelles recherches suggérant que la CRSC fait partie du spectre pachychoroïdien feront progresser la compréhension de la maladie, ce qui permettra d’offrir de meilleurs traitements aux patients atteints de CRSC.
Références
1. Zhang, X., Lim, C. Z. F., Chhablani, J., & Wong, Y. M. (2023). Central serous chorioretinopathy: updates in the pathogenesis, diagnosis and therapeutic strategies. Eye and Vision (London, England).
2. Moran CORE. (s/f). Utah.edu. ;https://morancore.utah.edu/section- 12-retina-and-vitreous/central-serous-chorioretinopathy-casereport/
3. Matet, A., Manassero, A., Daruich, A., Cassoux, N., & Behar-Cohen, F. (s/f). Diagnostics différentiels de la choriorétinopathie séreuse centrale. Cahiers-ophtalmologie.fr.
4. Hamzah, F., Shinojima, A., Mori, R., & Yuzawa, M. (2014). Choroidal thickness measurement by enhanced depth imaging and swept-source optical coherence tomography in central serous chorioretinopathy. BMC Ophthalmology,
5. Kaye, R., Chandra, S., Sheth, J., Boon, C. J. F., Sivaprasad, S., & Lotery, A. (2020). Central serous chorioretinopathy: An update on risk factors, pathophysiology and imaging modalities. Progress in Retinal and Eye Research, 79(100865)
6. Bousquet, E., Provost, J., Torres-Villaros, H., & Behar-Cohen, F. (2023). Choriorétinopathie séreuse centrale : une revue. Journal francais d’ophtalmologie, 46(7), 791–802.
7. Chhablani, J., Cohen, F. (2020). Multimodal Imaging-Based Central Serous Chorioretinopathy Classification Ophthalmology Retina 4 (11)
8. Chen, Z. J., Lu, S. Y., Rong, S. S., Ho, M., Ng, D. S.-C., Chen, H., Gong, B., Yam, J. C., Young, A. L., Brelen, M., Tham, C. C., Pang, C. P., & Chen, L. J. (2022). Genetic associations of central serous chorioretinopathy: a systematic review and meta-analysis. The British Journal of Ophthalmology, 106(11), 1542–1548.
9. Layikh, H., Saeed, S., & Attar, H. (2021). The relation between Helicobactor pylori gastrointestinal tract infection and central serous chorioretinopathy among patients in Al-Diwaniya province. Saudi Journal of Ophthalmology: Official Journal of the Saudi Ophthalmological Society, 35(2), 93.
10. Caillaux, V., Miere, A., Gherdaoui, F., & Souied, E. H. (n.d.). L’angio- OCT : l’angiographie sans colorant. Cahiers-Ophtalmologie.Fr. Retrieved January 16, 2024, https://www.cahiers-ophtalmologie.fr/ media/1bac600f2d4d6b01ecc810d49f190b97.pdf
11. Hwang, B.-E., Kim, J.-Y., Kim, R.-Y., Kim, M., Park, Y.-G., & Park, Y.-H. (2023). En-face optical coherence tomography hyperreflective foci of choriocapillaris in central serous chorioretinopathy. Scientific Reports, 13(1), 1–10.

